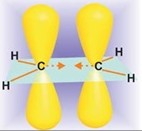
В 1942 г. Карл Циглер воспроизвел раннюю работу А. Воля по бромирование алкенов и показал, что реакция алкенов с N-бромсукцинимидом в CCl4, инициированная перекисями, является общим методом бромирования алкенов в так называемое аллильное положение — аллильное бромирование алкенов (аллильным называется атом углерода в α-положении по отношению к двойной связи). N-Бромсукцинимид (NBS) получается при взаимодействии сукцинимида (имида янтарной кислоты) с бромом в щелочной среде: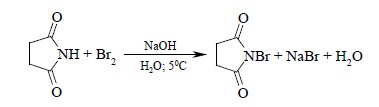
NBS селективно бромирует и циклические алкены только по аллильному атому углерода:
Как можно объяснить бромирование исключительно в аллильное положение и как объяснить образование при бромировании октена-1 сразу двух продуктов, из которых с одном произошло изменение положения двойной связи? Ответ на этот вопрос сводится к рассмотрению особой стабильности аллил-радикала. Бромирование алкенов по Циглеру с NBS представляет собой цепной радикальной процесс с участием атома брома. Атом брома образуется при фотолизе или термической гомолитической диссоциации молекулярного брома, образующегося в очень низкой концентрации из NBS и следов HBr, или за счет термического разложения NBS: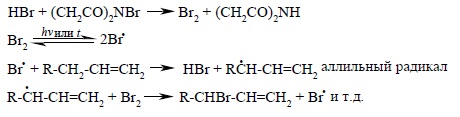
Направление радикального галогенирования определяется относительной стабильностью радикала, образующегося в качестве интермедиата (гл. 4). Бромирование алкенов в аллильное положение определяется более низкой энергией C – H-связи в аллильном положении по сравнению с энергией C – H-связи обычной метиленовой или метильной группы. Эти данные были приведены в главе 4, и для большей наглядности приведены на примере 4-метилциклогексена: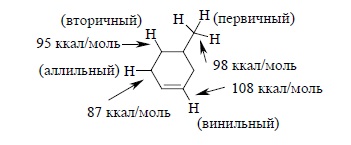
Из них следует, что аллильный радикал стабильнее вторичного алкильного радикала на ~8 ккал/моль, на 11 ккал/моль стабильнее первичного алкильного радикала и на 20 ккал/моль стабильнее винильного радикала. Циклогексен как симметричный алкен образует, естественно, только один продукт замещения водорода на бром в аллильном положении. Такие аллильные галогениды особенно важны для синтеза поряженных диенов при дегидрогалогенировании: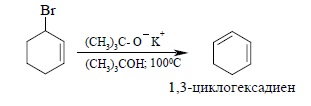
Вместо N-бромсукцинимада можно использовать N-хлорсукцинимид, который хлорирует алкены по аллильному положению. Реакцией, родственной аллильному галогенированию по Циглеру считается прямое газообразное хлорирование пропилена при 400 – 500ºС (Д.М. Львов, 184 г.):![]()
В настоящее время эта реакция лежит в основе промышленного способа получения хлористого аллила в больших количествах. В таких условиях присоединение хлора к двойной связи становится обратимой реакцией, где равновесие сильно смещено в сторону исходных реагентов. С этой реакцией успешно конкурирует прямое радикальное замещение водорода в аллильном положении: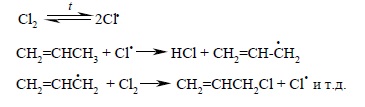
Аллилхлорид используется для получения эпихлоргидрина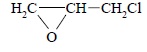
и других соединений с аллильной группой.
Таким образом, реакции радикального замещения водорода в аллильном положении, как и реакции радикального присоединения по двойной связи, столь же типичны для алкенов, как и процессы электрофильного присоединения по кратной связи.